锂电池简介
锂电池,是早期由爱迪生发明的一种由锂金属或锂合金为负极材料、使用非水电解质溶液的电池,其工作原理为一种Li+MnO2=LiMnO2的氧化还原反应。由于锂金属的化学特性非常活泼,使得其长期没有得到广泛应用,但现在随着科学技术的高速发展,锂电池逐渐成为主流。

锂电池的发展阶段
1、1970年代埃克森的M.S.WhitTIngham采用硫化钛作为正极材料,金属锂作为负极材料,制成首个锂电池。
2、1980年,J. Goodenough 发现钴酸锂可以作为锂离子电池正极材料。
3、1982年伊利诺伊理工大学(the Illinois InsTItute of Technology)的R.R.Agarwal和J.R.Selman发现锂离子具有嵌入石墨的特性,此过程是快速的,并且可逆。与此同时,采用金属锂制成的锂电池,其安全隐患备受关注,因此人们尝试利用锂离子嵌入石墨的特性制作充电电池。首个可用的锂离子石墨电极由贝尔实验室试制成功。
4、1983年M.Thackeray、J.Goodenough等人发现锰尖晶石是优良的正极材料,具有低价、稳定和优良的导电、导锂性能。其分解温度高,且氧化性远低于钴酸锂,即使出现短路、过充电,也能够避免了燃烧、爆炸的危险。
5、1989年,A.Manthiram和J.Goodenough发现采用聚合阴离子的正极将产生更高的电压。
6、1991年索尼公司发布首个商用锂离子电池。随后,锂离子电池革新了消费电子产品的面貌。
7、1996年Padhi和Goodenough发现具有橄榄石结构的磷酸盐,如磷酸锂铁(LiFePO4),比传统的正极材料更具优越性,因此已成为当前主流的正极材料。

锂电池的分类
1、按锂电池的外型分:方型锂电池(如常用的手机电池电芯)和柱形锂电池(如18650);
2、按锂电池外包材料分:铝壳锂电池,钢壳锂电池,软包电池;
3、按锂电池正负极材料(添加剂)分:沽酸锂(LiCoO2)电池或锰酸锂(LiMn2O4),磷酸铁锂电池,一次性二氧化锰锂电池;另一种分法:锂离子LIB,聚合物PLB
4、不同的性能用途方面分:
一次性锂电池---锂锰电池--扣式3伏电池
高容量(高平台)锂电池--用在手机数码产品上
高倍率锂电池;---用在电动车和电动工具上及飞机模型
高温锂电池;---矿灯,室上灯饰,机器内置后备电源;
低温锂电池;---室外环境,北方(冬天)南极;
5、锂电池还分成两类:不可充电的和可充电两类。

锂电池的结构
锂电池在结构上主要有五大块:正极、负极、电解液、隔膜、外壳与电极引线。
目前较为常用的锂电池材料有钴酸锂、镍酸锂以及锰酸锂。用得最多的材料是钴酸锂,循环性能好,制造也方便,缺点是钴化合物价格较贵。镍酸锂的因为性质不稳定,制造困难,通常用得较多的是钴酸锂掺杂镍的化合物,又称镍钴酸锂。锰酸锂也是非常好的材料,在高温下锰酸锂的衰减比较快等诸多原因,目前应用多数还停留在实验室阶段。
锂电池的结构主要分卷绕式和层叠式两大类。液态锂电池采用卷绕结构,聚合物锂电池则两种都有。卷绕式将正极膜片、隔膜、负极膜片依次放好,卷绕成圆柱形或扁柱形,主要以SANYO、TOSHIBA、SONY、ATL为代表。层叠式则将正极、隔膜、负极、隔膜、正极这样的方式多层堆叠。将所有正极焊接在一起引出,负极也焊成一起引出,主要以ATL为代表。
锂电池工作原理
1、充电时
在电场的驱动下锂离子从正极晶格中脱出,经过电解质,嵌入到负极晶格中。
充电开始时,应先检测待充电电池的电压,如果电压低于3V,要先进行预充电,充电电流为设定电流 的1/10,一般选0.05C左右。电压升到3V后,进入标准充电过程。标准充电过程为:以设定电流进行恒流充电,电池电压升到4.20V时,改为恒压充电,保持充电电压为4.20V。此时,充电电流逐渐下降,当电流下降至设定充电电流的1/10时,充电结束。
一般锂电池充电电流设定在0.2C至1C之间,电流越大,充电越快,同时电池发热也越大。而且,过大的电流充电,容量不够满,因为电池内部的电化学反应需要时间。就跟倒啤酒一样,倒太快的话会产生泡沫,反而不满。
术语解释:充放电电流一般用C作参照,C是对应电池容量的数值。电池容量一般用Ah、mAh表示,如M8的电池容量1200mAh,对应的C就是1200mA。0.2C就等于240mA。
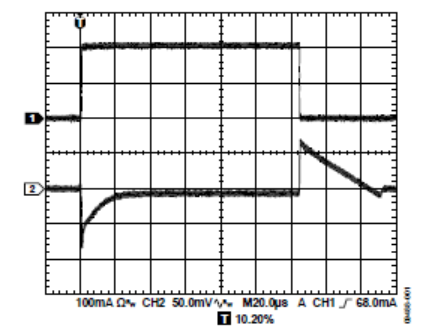
下面是锂电池典型充电曲线图:

2、放电时
过程正好相反锂离子返回正极,电子通过用电器由外电路到达正极与锂离子复合。
从典型放电曲线图上可以看出,电池放电电流越大,放电容量越小,电压下降更快。